Метаданни
Данни
- Включено в книгата
- Оригинално заглавие
- The World of Carbon, 1958 (Пълни авторски права)
- Превод от английски
- Сашо Чорбаджиев, 1987 (Пълни авторски права)
- Форма
- Научен текст
- Жанр
- Характеристика
-
- Няма
- Оценка
- 5,8 (× 14 гласа)
- Вашата оценка:
Информация
- Сканиране
- gogo_mir (2012 г.)
- Разпознаване и корекция
- Ripcho (2012 г.)
- Допълнителна корекция
- waterjess (2015)
Издание:
Айзък Азимов. Светът на въглерода
Американска, първо издание
Преводач: Сашо Чорбаджиев
Редактор: Румяна Бикс
Художник: Слав Даскалов
Художествен редактор: Виктор Паунов
Технически редактор: Василка Стефанова-Стоянова
Коректор Анна Сребрева
Печатни коли: 11,50
Издателски коли: 7,45
УИК 8,75
Издателски №29506
Формат: 32/70/100
ДИ „Наука и изкуство“ — София, 1987 г.
ДП „Стоян Добрев — Странджата“ — Варна
История
- — Добавяне
- — Корекция
Газирана вода и спанак
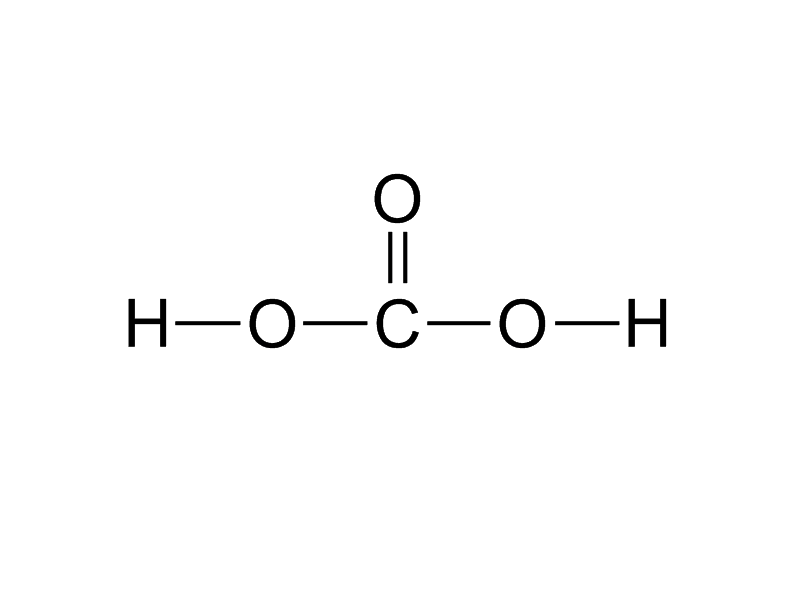
Свободната връзка на карбоксилната група може да бъде свързана с хидроксилна група по следния начин:
Получава се съединението въглеродна киселина.
Въглеродната киселина е твърде нестабилна. Тя не може да съществува в чисто състояние. (Ако се опитате да я получите в чист вид, молекулите й се разпадат до по-простите молекули на водата и въглеродния двуокис.) Тя може да съществува в разтвор, т.е. смесена с вода, но дори и тогава повечето молекули се разпадат.
Газираната вода е вода с разтворен в нея въглероден двуокис. Въглеродният двуокис (който е газ) е разтворен под налягане, за да се смеси по-голямо количество от него с водата. Когато при отварянето на бутилката налягането се понижи, излишният въглероден двуокис се отделя във вид на мехурчета. Малкото количество въглеродна киселина, образувано от свързването на малко въглероден двуокис с вода, придава на газираната вода приятен резлив вкус.
Молекулата на въглеродната киселина може да загуби и двата водородни атома. Ако се отдели един водороден йон, остава бикарбонатен (кисел карбонатен, хидрогенкарбонатен) йон. Вторият водороден атом се отстранява около хиляда пъти по-трудно от първия. Когато и той се отстрани, остатъкът се нарича карбонатен йон. В кръвния поток на човека, а и в самите тъкани има въглеродна киселина, бикарбонатни йони и разтворен въглероден двуокис, но няма карбонатни йони.
Бикарбонатният и карбонатният йон често се съединяват с йоните на някои метали. Получените съединения, макар и да съдържат въглерод, приличат на неорганичните. Например калциевият[1] карбонат е минерал, обикновено наричан варовик. Той се среща също и в много по-красивата разновидност, наречена мрамор. Живите организми могат да произвеждат калциев карбонат. Той изгражда скелета на коралите[2], както и черупките на миди, стриди, охлюви и птичи яйца.
Натриев карбонат може да се намери в много домакинства под обикновеното име сода за пране. Още по-вероятно е там да намерите натриев бикарбонат, който обикновено се нарича сода за хляб или сода за пиене, или сода бикарбонат.
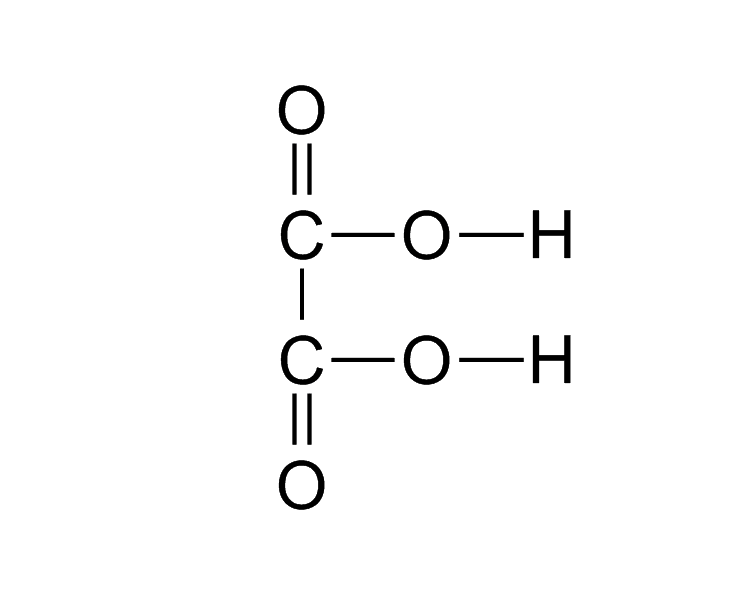
Свободната връзка на една карбоксилна група може да бъде свързана с втора карбоксилна група. Получава се съединението оксалова киселина:
Името й произлиза от латинското име на киселеца[3], в който се съдържа.
Оксаловата киселина може да загуби първо един водороден йон, след това и втори подобно на въглеродната киселина. Когато се отделят и двата водородни йона, получава се остатък, наречен оксалатен йон. Той може да се свърже с калциев йон и да образува калциев оксалат.
Калциевият оксалат е много неразтворим и това го прави много полезен понякога за химиците. Понякога те се интересуват какво количество калциеви йони съдържа дадено вещество. Тогава разтварят веществото във вода. (Ако е необходимо, предварително го обработват по такъв начин, че да го направят разтворимо.) Към разтвора прибавят известно количество някое съединение, което съдържа оксалатен йон в молекулата си. Оксалатният йон незабавно се свързва с всички (или почти всички) налични калциеви йони. Калциевият оксалат, понеже е неразтворим, се утаява; т.е. напуска разтвора във вид на фин бял прах и пада на дъното на съда. Химикът може да отдели този прах и да го претегли точно. От теглото му може да каже какво количество калциеви йони е имало в пробата от първоначалната смес. Това е един пример от химичния анализ.
Понякога се образува калциев оксалат и при не така благоприятни обстоятелства. Организмът образува оксалатен йон в малки количества, като част от нормалното функциониране на „химията“ му. Като последица в урината се появява известно количества оксалатни йони[4]. Към урината непрекъснато се насочва и значително количество калциеви йони. Следователно се образува калциев оксалат. Обикновено малките кристали калциев оксалат някак си успяват да не се слепят помежду си. (Химиците не са сигурни как точно става това.) При малък брой хора обаче нещо не е наред и кристалите се залепват един с друг и образуват малък твърд „камък“. Такива камъни могат да запушат каналчетата, които излизат от бъбреците. Тези камъни в бъбреците[5] могат да бъдат извънредно болезнени и понякога е необходима хирургическа намеса, за да се отстранят.
Някои храни — например спанак и ревен — съдържат големи количества оксалова киселина или оксалатни йони. Фактически ревеновите листа съдържат толкова много оксалат, че са отровни. Стеблата обаче са добри. Спанакът, разбира се, се предполага, че е „полезен“. Но наличието на оксалова киселина в спанака го прави не така полезен, както мислят повечето хора. Оксаловата киселина свързва калция, който в противен случай може да се използува за изграждането на костите. Част от желязото, което се съдържа в спанака, също се свързва с оксалова киселина и не може да се използува от организма.
Едно по-сложно съединение с две карбоксилни групи е адипиновата киселина. Тя има четири въглеродни атома между двете групи и се използува за получаването на найлон.